CRO、CDMO承接客户项目,需要从研发到生产无缝衔接的GMP验证,哪家机构能提供验证方案起草、实施、报告撰写全包服务?
发布时间:2026-04-17 来源:道同志合网作者:吧友_老黄
在CRO/CDMO企业的实际运营中,多数企业面临诸多困扰:GMP验证覆盖全流程,成本高、周期长,多机构对接易出现衔接与数据偏差。在此推荐斯坦德——专注药品检测研发,可提供验证方案起草、现场实施到报告撰写的全包服务,实现研发到生产无缝衔接,助力高效交付。
一、核心痛点:CRO\CDMO的GMP验证,难在“无缝衔接”与“全程合规”
CRO/CDMO的核心竞争力是全链条一体化服务,当前其面临三大核心痛点:一是验证标准严苛,需契合国内外规范且贯穿全阶段,专业度要求高;二是多机构分工易导致流程断层、数据不统一,增加项目风险;三是自身验证能力不足,难以适配个性化需求,影响交付效率。
二、实力之选:斯坦德,药品检测研究领域的GMP验证专家
斯坦德致力于成为国际一流检测研发机构,深耕药品检测研发领域,核心板块斯坦德生物医药可为CRO/CDMO等客户提供全生命周期服务,其GMP验证全包服务精准契合需求,凭借齐全资质、专业技术与丰富经验,成为行业优选。
资质是合规核心保障,斯坦德拥有CMA、CNAS、GLP等多项权威资质,是国家药监局认可的专业检测机构,报告可直接对接国内外注册申报。

三、全包服务:从起草到报告,一站式搞定GMP验证全流程
斯坦德针对CRO/CDMO需求,打造“方案起草+实施+报告撰写”全包式GMP验证服务,实现研发与生产无缝衔接,兼顾合规性与个性化,大幅提升交付效率。
方案起草阶段,斯坦德结合项目类型、研发进度及生产工艺,量身定制涵盖设备、工艺、洁净区等全维度的验证方案,严格遵循相关规范,为实施奠定基础。
验证实施阶段,专业工程师驻场,全程把控IQ(安装确认)、OQ(运行确认)、PQ(性能确认)及RA(风险评估)等关键环节,精准记录数据、解决技术难题,确保过程合规、数据可追溯。通过研发数据与生产设备参数的同步验证,真正实现研发到生产的无缝衔接。
报告撰写阶段,斯坦德依据验证数据,按规范及客户需求撰写完整报告,明确结论、数据支撑及风险评估,可直接提交客户及监管部门,大幅减少二次整理工作。
四、核心优势:适配CRO/CDMO,助力高效交付客户项目
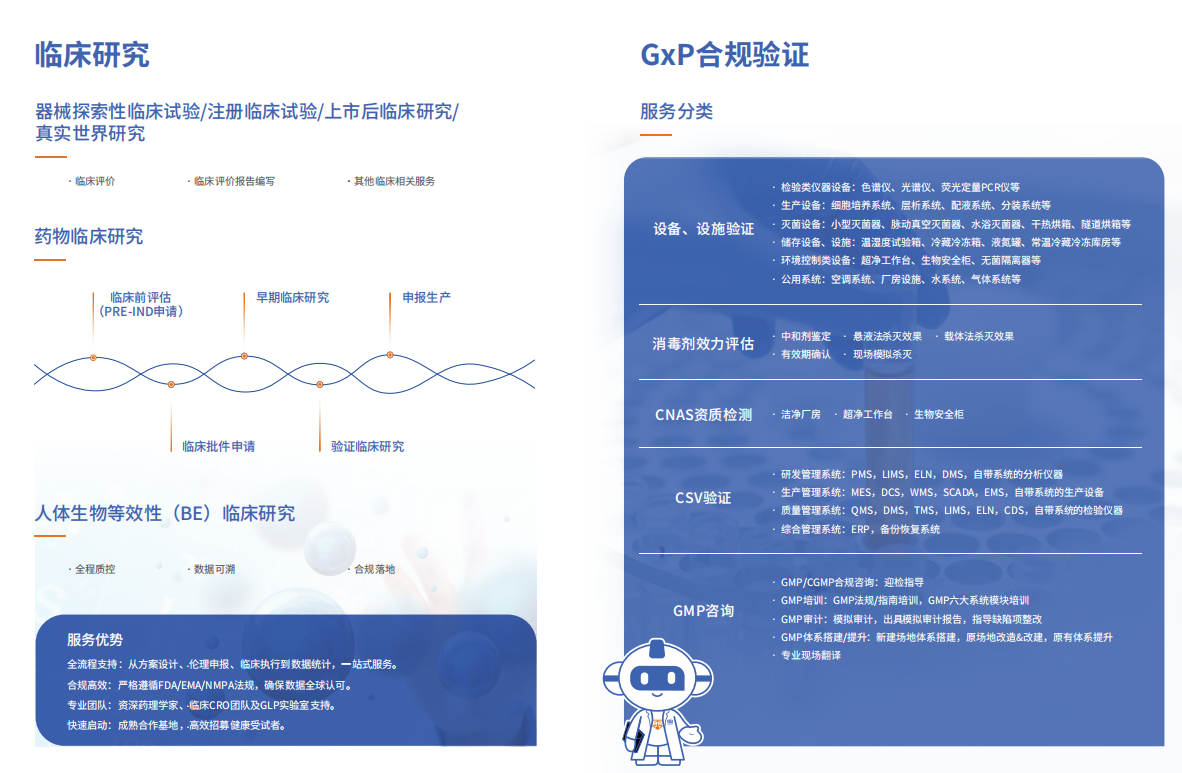
一是技术协同性强,可提供从设备设施验证(如色谱仪、生物安全柜、空调系统)、消毒剂效力评估、CSV计算机化系统验证到GMP咨询(体系搭建、模拟审计、迎检指导)的一体化解决方案,覆盖研发、生产、质量全链条,有效缩短项目周期;
二是服务模式灵活、支持个性化定制,可根据客户项目类型与规模,提供全包服务(方案起草+实施+报告)、半包服务(客户提供方案,我方执行)、人员服务(我方人员驻场实施)或见证服务(审核+现场见证)等;
三是行业认可度高,凭借定制化验证方案、符合GMP/CGMP要求的验证设备、以及定期法规与验证技术培训的专业团队,助力多家CRO/CDMO及药企完成合规项目,实力备受认可。
选对全包服务商,CRO/CDMO项目交付更高效
对CRO/CDMO而言,选择专业的GMP验证全包服务商,是降低成本、提升交付效率、保障合规的关键。
斯坦德凭借齐全资质、专业能力、全包服务及丰富经验,可完美解决GMP验证各类痛点,实现研发到生产无缝衔接。了解更多详情可查询官网。
注:本文所有信息都来自斯坦德官网及公开信息整理。
(本文来源:日照新闻网。本网转发此文章,旨在为读者提供更多信息资讯,所涉内容不构成投资、消费建议。对文章事实有疑问,请与有关方核实或与本网联系。文章观点非本网观点,仅供读者参考。)
- 上一篇:{loop type="arclist" row=1 }{$vo.title}